Seis preguntas para diferenciar las vacunas de Pfizer y Moderna
Las dos tienen en común que utilizan la tecnología de ARN mensajero, pero tienen efectividades distintas y necesitan de temperaturas de refrigeración disímiles.
Las dos primeras vacunas contra el Covid-19 han proporcionado noticias positivas en la búsqueda para poner fin a la pandemia. Los alentadores resultados de los ensayos de etapa final de Pfizer Inc. y Moderna Inc. dejaron la vara alta a sus rivales, como AstraZeneca Plc, que se espera que dé a conocer pronto sus propios resultados clave.
Es probable que los datos aumenten la confianza en que más vacunas funcionarán y que el mundo pronto encontrará una manera de controlar el coronavirus. Esto es lo que sabemos sobre las dos vacunas.
¿Cómo se comparan los resultados?
Moderna dijo este lunes 16 de noviembre que su vacuna tenía una efectividad de 94,5% en un análisis preliminar. Eso se compara favorablemente con el elevado nivel de efectividad alcanzado una semana antes por Pfizer y su socio, BioNTech SE. La vacuna creada por la empresa estadounidense junto con la compañía alemana resultó tener una efectividad mayor a 90%. Los datos de Moderna mostraron que los efectos secundarios fueron generalmente de corta duración y no hubo preocupaciones de seguridad significativas, mientras que no se desarrollaron casos graves de Covid entre los participantes del ensayo que recibieron la vacuna. Los reguladores estadounidenses lanzaron a principios de este año una guía que decía que cualquier vacuna debería tener al menos una efectividad de 50%.
¿Qué tienen en común las dos vacunas?
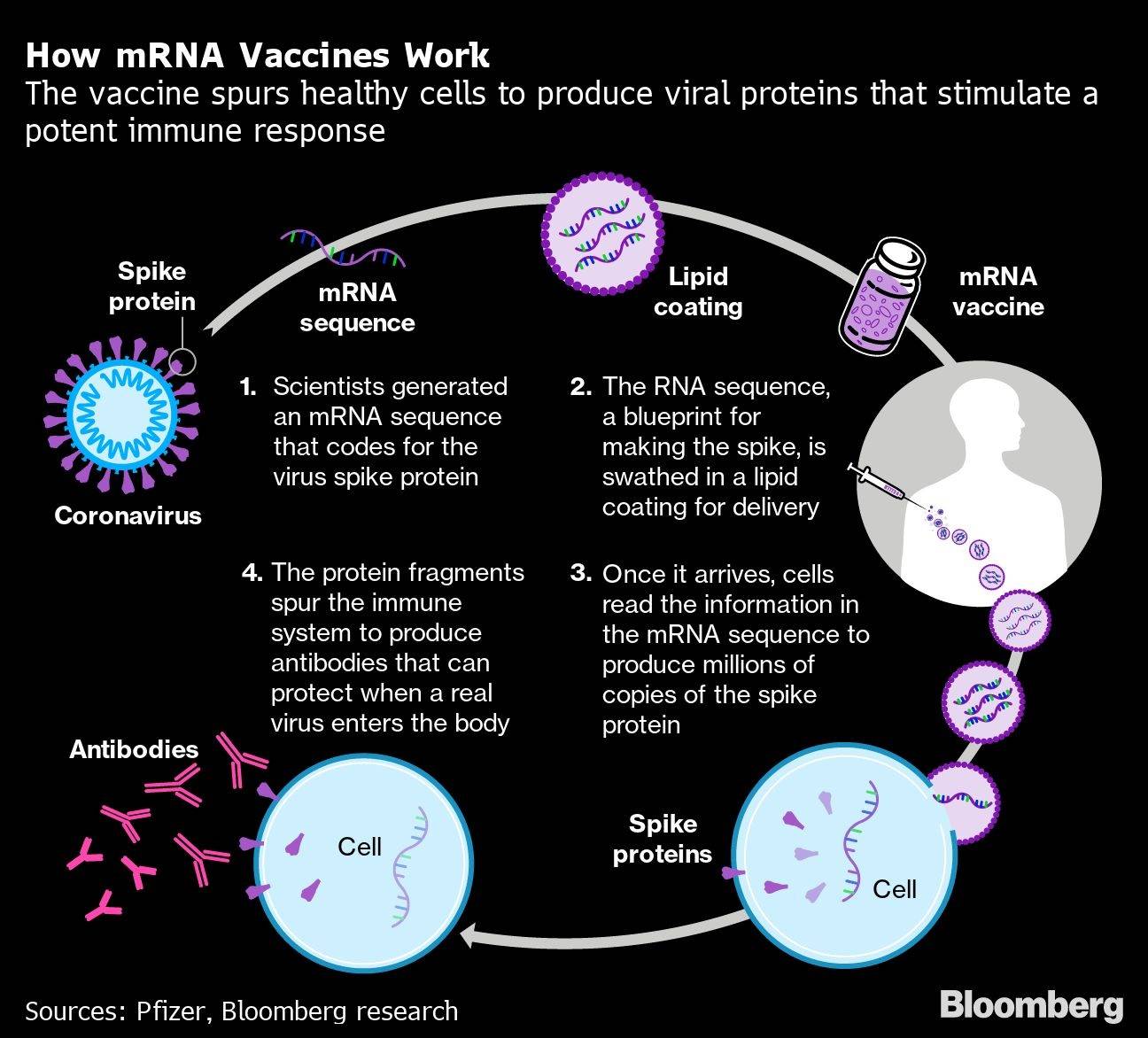
Ambas vacunas se basan en una tecnología llamada ARN mensajero que nunca se ha utilizado antes para desarrollar una vacuna aprobada. El enfoque está diseñado para transformar las propias células del cuerpo en fábricas de vacunas. Las vacunas instruyen a las células a hacer copias de la proteína espiga del coronavirus, estimulando la creación de anticuerpos protectores.
¿En qué se diferencian?
Moderna recibió US$ 955 millones del programa Operation Warp Speed de Estados Unidos. Pfizer ha dicho que no recibió ningún financiamiento federal para desarrollar su vacuna, aunque BioNTech obtuvo 375 millones de euros (US$ 444 millones) en ayuda del gobierno alemán. Aun así, Pfizer ha llegado a un acuerdo de suministro con EE.UU. por valor de casi US$ 2.000 millones. Estados Unidos ha acordado pagar hasta US$ 1.530 millones para comprar suministros de la vacuna de Moderna.
¿Cuáles son los desafíos de almacenamiento y distribución?
Una vez que se aprueben las vacunas, el esfuerzo por inmunizar a cientos de millones de personas deberá superar una serie de obstáculos. El almacenamiento y distribución de algunos de los productos es complejo. La vacuna de Pfizer requiere un almacenamiento ultrafrío hasta unos días antes de su uso, pero se puede conservar a la temperatura del refrigerador hasta por cinco días. Moderna, por su parte, señaló que nuevos datos muestran que su vacuna es estable a la temperatura del refrigerador durante 30 días, mucho más que los siete días estimados previamente. Puede conservarse en congeladores durante un período más largo y no necesita las instalaciones especiales requeridas para la vacuna de Pfizer.
¿A dónde llegarían primero las vacunas?
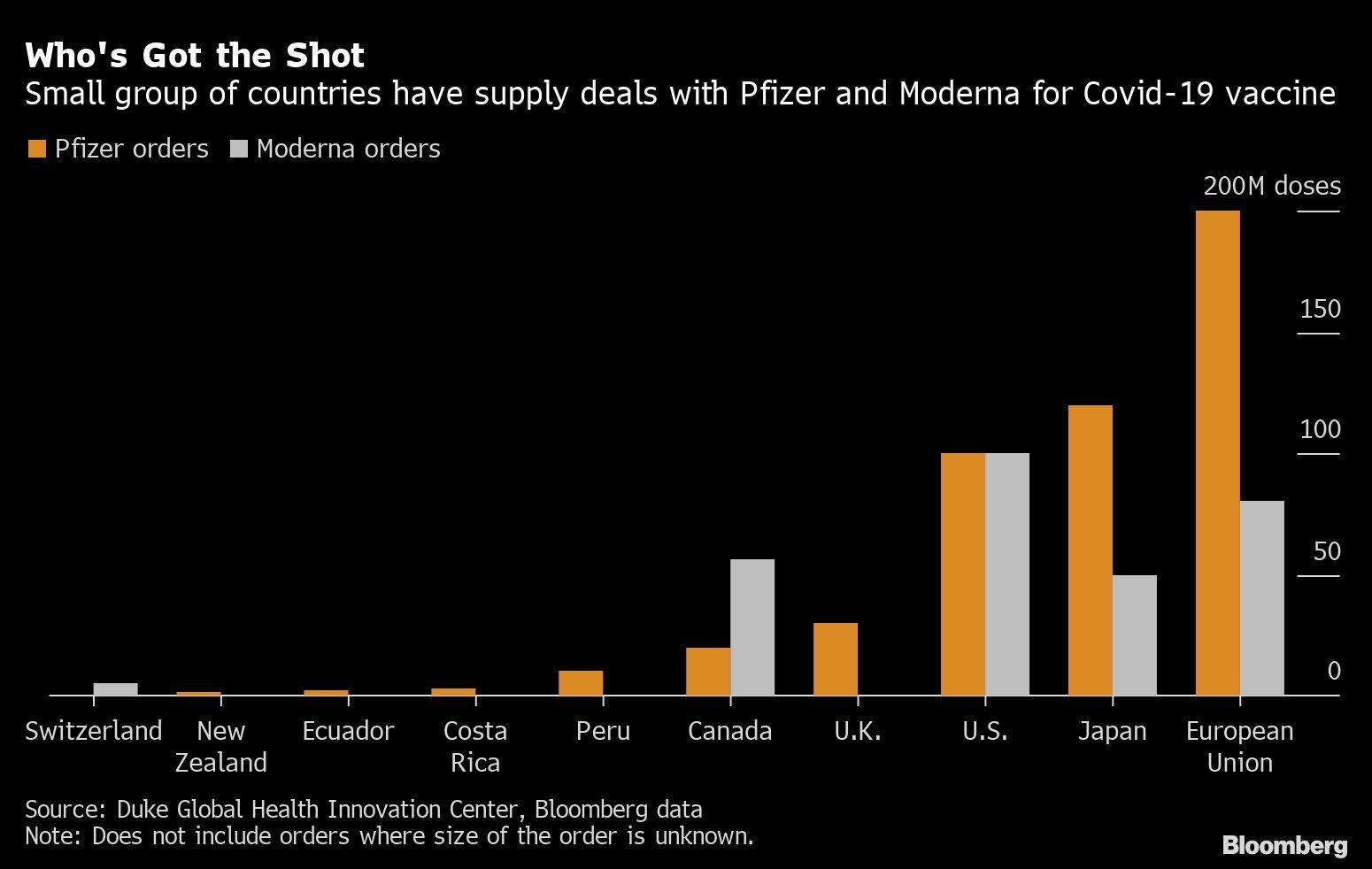
Inicialmente, se espera que la demanda mundial de vacunas supere con creces los suministros a pesar de los importantes esfuerzos para acelerar la producción. Moderna ya ha alcanzado acuerdos para suministrar 100 millones de dosis a EE.UU. y 80 millones a la Unión Europea, entre otros. Pfizer y BioNTech también tienen sus propios acuerdos para cientos de millones de dosis.
¿Cuándo podrían estar listas para ser suministradas?
Los resultados son preliminares, pero se espera que tanto Moderna como Pfizer soliciten la autorización de uso de emergencia de la Administración de Alimentos y Medicamentos de Estados Unidos si una revisión adicional demuestra que sus vacunas son seguras. Moderna dijo que podría solicitar la autorización de los reguladores en las próximas semanas. Pfizer espera tener dos meses de datos de seguimiento de seguridad en la tercera semana de noviembre. Si todo va bien, Pfizer podría solicitar una autorización en EE.UU. este mes.
